H2O2 + Fe(III)-E → H2O + O=Fe(IV)-E(.+)
H2O2 + O=Fe(IV)-E(.+) → H2O + Fe(III)-E + O2
其中,“Fe()-E”表示结合在酶上的血红素基团(E)的中 心铁原子(Fe)。Fe(IV)-E(.+)为Fe(V)-E的一种共振形式,即铁原子并没有完全氧化到+V价,而是从血红素上接受了一些“支持电子”。因而,反应式中的血红素也就表示为自由基阳离子(.+).
过氧化氢进入活性位点并与酶147位上的天冬酰胺残基(Asn147)和74位上的组氨酸残基(His74)相互作用,使得一个质子在氧原子间互相传递。自由的氧原子配位结合,生成水分子和Fe(IV)=O。Fe(IV)=O与第 二个过氧化氢分子反应重新形成Fe(III)-E,并生成水分子和氧气。[活性中 心铁原子的反应活性可能由于357位上酪氨酸残基(Tyr357)的苯酚基侧链的存在(帮助Fe(III)氧化为Fe(IV))而得以提高。反应的效率可能是通过His74和Asn147与反应中间体作用而得以提高。该反应的速率通常可以通过米氏方程来确定。
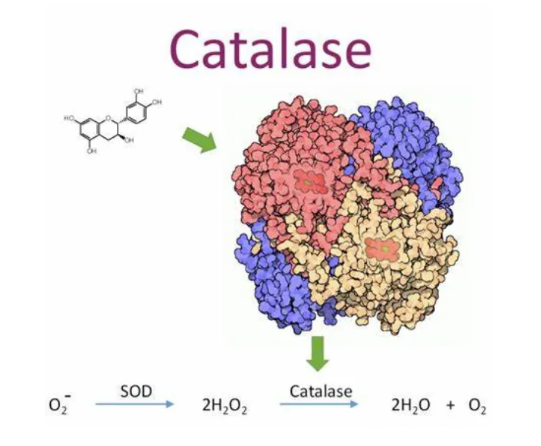
H2O2 + H2R → 2H2O + R
同样,具体的反应机制还不清楚。
任何重金属离子(如硫酸铜中的铜离子)可以作为过氧化氢酶的非竞争性抑 制剂。另外,剧毒性的氰化物是过氧化氢酶的竞争性抑 制剂,可以紧密地结合到酶中的血红素上,阻止酶的催化反应。
处于过氧化状态的过氧化氢酶中间体的三维结构已经获得解析,可以在蛋白质数据库中检索到。
 咨询热线:0632-3279666
咨询热线:0632-3279666  城市分站
城市分站  联系我们
联系我们 


 邮箱:ren6669@126.com
邮箱:ren6669@126.com  电话:0632-3279666
电话:0632-3279666 
 地址:山东省枣庄市市中区孟庄镇工业园区移山路6号
地址:山东省枣庄市市中区孟庄镇工业园区移山路6号 
